Ribosome ProfilingGenome-wide survey of translational control in microgravity

| 宇宙利用/実験期間 | 2020年 ~ 2021年 |
|---|---|
| 研究目的 | 地球上の生物は40億年の歴史の進化の中で地球上の重力に適応しました。しかし、細胞が重力に対してタンパク質を合成する過程である「翻訳」をどのように制御しているかについては全く理解されていません。本研究では、重力による翻訳制御についてリボソームプロファイリング法を用いて明らかにします。 |
| 宇宙利用/実験内容 | 細胞は、栄養やストレスなどの環境に応答してタンパク質を合成する過程である「翻訳」を制御することにより迅速に環境変化に対応することが広く知られています。本研究では、国際宇宙ステーション(ISS)内の「きぼう」日本実験棟で培養したヒト培養細胞に対してリボソームプロファイリング法で解析することで、微小重力環境下での翻訳の変化のスナップショットを網羅的かつ定量的に調べます。 |
| 期待される利用/研究成果 | 重力への適応機構の分子メカニズムの解明は生命科学のフロンティアです。生命科学史上、微小重力が細胞の「翻訳」に与える影響を網羅的に解析した例はなく、本提案実験は生命科学の歴史に残る研究になります。微小重力下で生じる加齢様症状との関連を示すことで、基礎科学、産業創出、また医学の分野で大きな効果が期待されます。 |
| 関連トピックス |
|
|
詳細
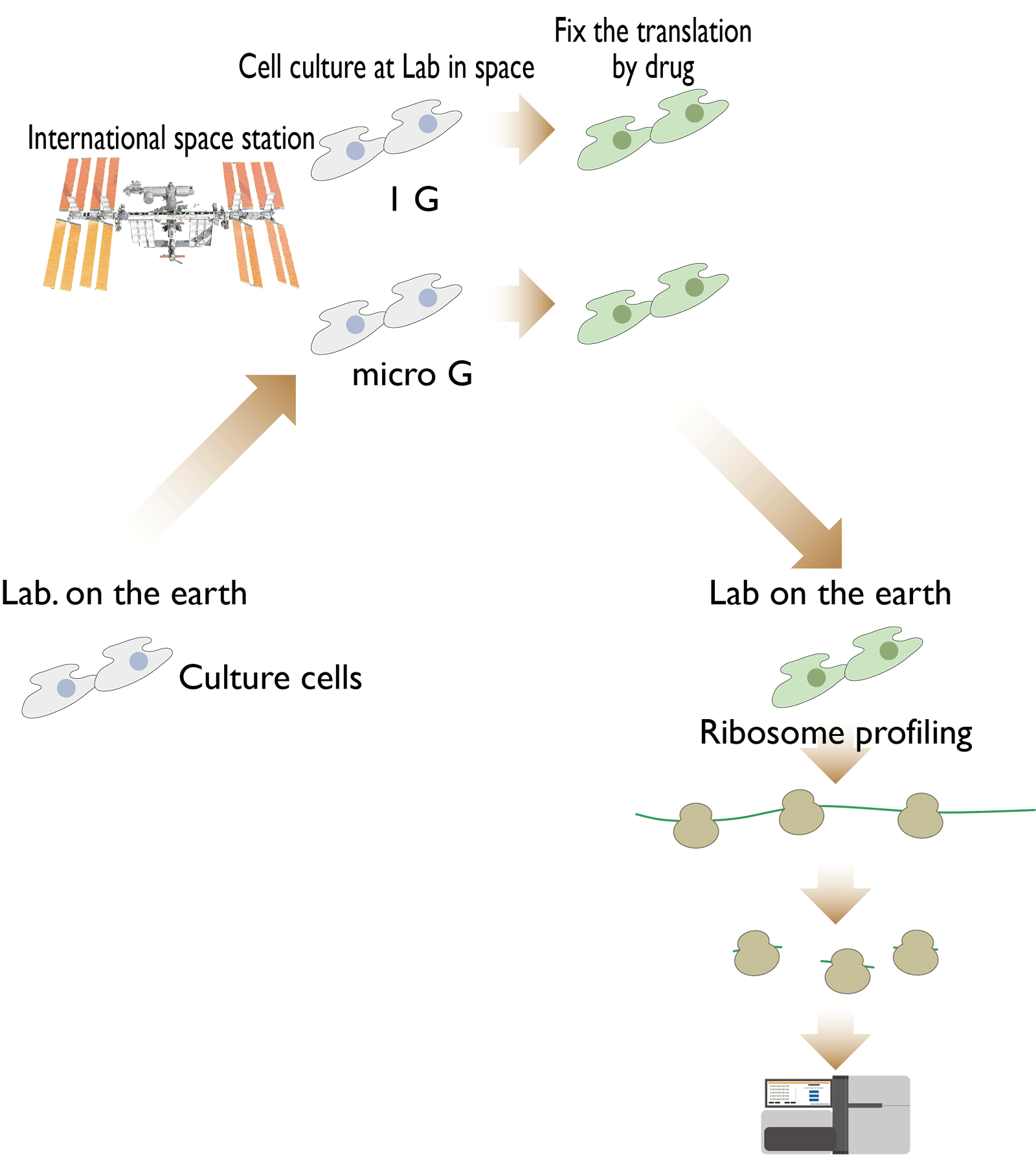
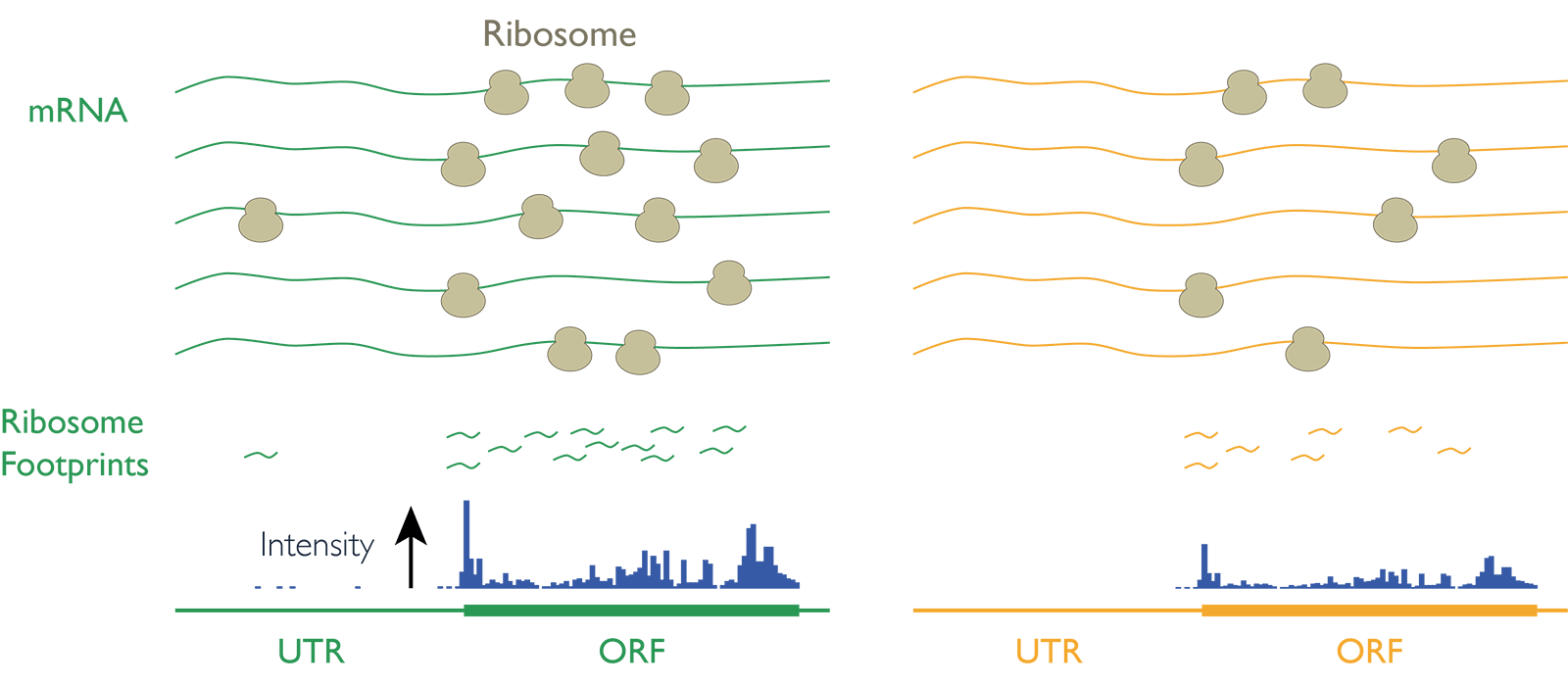
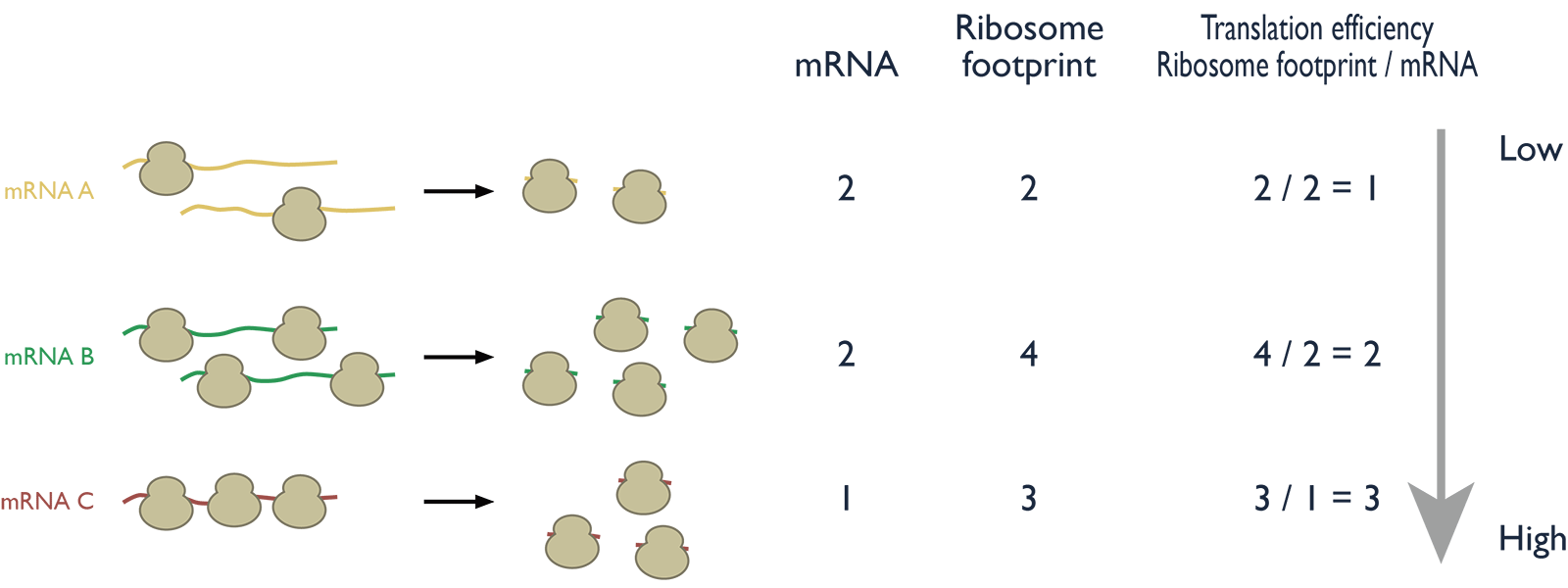
要旨栄養やストレスなどに応答するために、細胞はタンパク質を合成する過程である「翻訳」を制御することにより迅速に環境変化に対応することが広く知られています。重力は地上の生物にとって当たり前にある環境要素ですが、細胞がどのように重力に応答しているか、という点は驚くべきほどよくわかっていません。本研究では、細胞が微小重力にどのように応答し、「翻訳」を制御するかという点を明らかにすることを目的としています。微小重力環境下での翻訳状態の変化のスナップショットを網羅的かつ定量的に調べるために、私たちが得意とするリボソームプロファイリングと呼ばれる手法を用います。宇宙実験では、ISS内の「きぼう」で、微小重力環境下でヒト培養細胞を培養します(図1)。これを地上に持ち帰りリボソームプロファイリングを行います。それによって微小重力がどのようなタンパク質の翻訳効率にどの程度、影響を与えるかを一網打尽に解析します。 実験の概要本研究では、「微小重力下で特異的な翻訳制御が細胞内で生じる」という仮説を立て、これを検証します。ISS内の「きぼう」に設置された細胞培養装置(CBEF)を用いて、微小重力下(以下µGと表記する)でヒト培養細胞を培養します。比較対象のために同じくCBEF内の人工重力装置を用いてヒト培養細胞を培養し、地上と同じ1Gを再現します。この2つの条件で培養した細胞を比較することで、微小重力下で生じる翻訳の差を検証します。培養した細胞は、化学固定し、その後地上に持ち帰ります。 細胞の中では、タンパク質の設計図である遺伝子(DNA)の情報を基にmRNA(メッセンジャーRNA)が複製されます。さらにmRNAの遺伝暗号が読み取られタンパク質がつくられます。タンパク質はアミノ酸が多数連なってできています。このアミノ酸の並びはmRNAに遺伝暗号として記録されていてます。遺伝暗号は、塩基(アデニン=A、ウラシル=U、グアニン=G、シトシン=C)の並び順をアミノ酸の並び順に変換する規則のことです。例えば、アミノ酸の1種のトリプトファンは、3つの塩基の並び順"UGG"で表現されます。翻訳は、遺伝暗号に従ってmRNAに記録されたアミノ酸の並び順を1つ1つ読み解き、タンパク質を合成する過程のことです。この翻訳を担う分子実態(細胞内の小さな装置)がリボソームで、リボソームはmRNAと結合し、遺伝暗号の解読と同時にタンパク質を合成します。 リボソームプロファイリングは、塩基配列を解析する次世代シークエンサーを用いてmRNAに結合しているリボソームの数と結合位置を検出する新しい解析手法です(図2)。また、今回の実験では、同じく次世代シークエンサーを用いたRNA-Seqと呼ばれる解析手法を用いてmRNAの種類と数をカウントします。2つのデータを用いると1つ1つのmRNAの翻訳の効率を計算することができます。この翻訳効率をµGと1G環境下で比較し、どのmRNAの翻訳効率が増減するか、俯瞰します(図3)。これらのデータの中から、µG環境下で翻訳効率が変化するmRNAを抽出します。軌道上での実験は宇宙線の影響も考えられるため、得られた結果が宇宙線によらないか検証するため地上1Gで比較します。 期待される成果微小重力への適応機構の分子メカニズムの解明は生命科学のフロンティアです。生命科学史上、微小重力が細胞の「翻訳」に与える影響を網羅的に解析した例はなく、本提案実験は生命科学の歴史に残る研究となります。さらに、本研究は、ゲノムワイドな網羅性を有しているため、得られたデータから微小重力およびそれに付随する細胞の老化で変化するマーカー遺伝子(老化等に細胞の変化に対して鋭敏に応答する代表的な遺伝子)を同定することができます。それらマーカー遺伝子の増減を簡便に検出できるキットや試薬の創出が見込まれれば科学的イノベーションだけではなく、産業や医学への貢献も期待されます。また、マーカー遺伝子を制御することを通じて細胞の老化を遅らせるといった効果を狙った薬剤などの開発をなどの医療、産業的波及効果も期待されます。本研究の成果は基礎科学、産業創出、また医学の分野で大きな効果が期待される高い発展性があります。 |
|